| 研究期間 | 2021/4/1 - 2024/3/31 |
| 研究課題名 | 【終了】リモートプラズモニクスによる表面増強ラマン散乱を応用した、新しい慢性炎症性皮膚疾患の評価法の開発 |
| カテゴリー | 全てのクラスター、研究クラスター一覧、登録クラスター、医学、終了した研究クラスター、基礎、臨床、工学、光応用、バイオ、栄養、食品 |
| SDGs | 3.保健 9.イノベーション 17.実施手段 |
| 応募課題 | |
| クラスター長氏名 | 髙成 広起(ポストLEDフォトニクス研究所、医光融合研究部門、特任講師) |
| 所属する研究者氏名 | 南川丈夫(ポストLEDフォトニクス研究所 ポストLEDフォトニクス研究部門 准教授) 山本圭(大学院社会産業理工学研究部 生物資源産業学域 生体分子機能学分野 准教授) 異島優(大学院医歯薬学研究部 薬学域 薬物動態制御学分野 准教授) 清水真祐子(大学院医歯薬学研究部 医学域 疾患病理学分野 助教) |
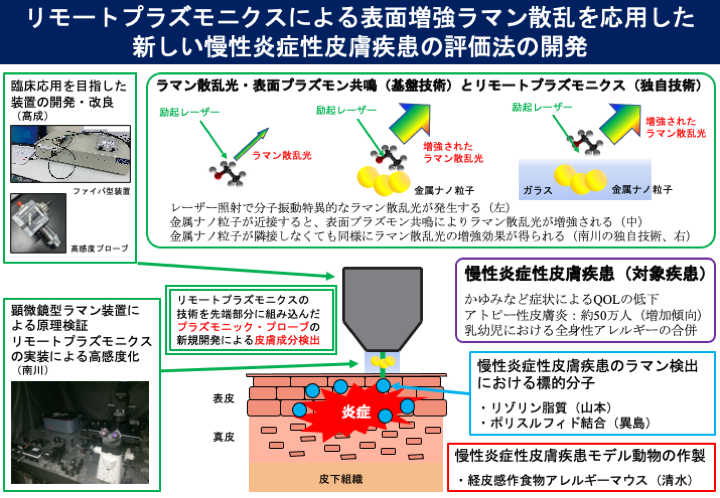
| 研究概要 | [背景]人体は常に外界からの刺激に曝露されており、皮膚は外界刺激に対するバリアとして働く。皮膚バリア機能の喪失を起点に、アトピー性皮膚炎などの慢性炎症性皮膚疾患や、特に乳幼児においては食物アレルギーが生じる。これらのアレルギー疾患の治療には、表皮の状態をリアルタイムに的確に評価でき、かつ患者に負担のない測定技術が求められている。 [研究開発の概要]研究代表者の高成は南川と協働でラマン分光法の臨床応用を目指した研究を行っている。ラマン分光光度法はレーザー照射による分子種特異的な散乱光の検出を可能とする非侵襲非標識観察技術であり、臨床応用を行ううえで皮膚は最も魅力のある対象臓器である。しかし生体由来のラマン散乱光は極めて微弱で夾雑なデータを含むため、いかに高感度に生体由来のラマン散乱光を検出するかが問題となっている。南川は独自技術として表面プラズモン共鳴現象を基盤としたリモートプラズモニクスによるラマン散乱光の増強を応用して、臨床における微量成分の非破壊・非標識検出技術の確立を目指している。 皮膚は生体防御の最前線の臓器であり、皮膚バリア機能の喪失はアトピー性皮膚炎などの慢性炎症性皮膚疾患や食物アレルギーを引き起こす要因と考えられている。徳島大学内では、異島が表皮角質蛋白中のポリスルフィド結合が表皮の抗酸化作用に関与する基礎研究を推進し、山本は表皮角質のリゾリン脂質(リゾプラズマローゲン)が慢性皮膚炎症を惹起するバイオマーカーとなることをヒトおよびマウスを用いて証明し、これらの対象分子が皮膚疾患を評価する非侵襲診断に活用できることを提唱してきた。また、清水は経皮感作アレルギーマウスを用いて食物アレルギーを抑制する機能性成分の基礎研究を展開してきた。 本研究クラスターでは、異なる研究バックグラウンド(医学、理工学・光学、薬学、脂質生物学、栄養学)で実績のある研究者を、「皮膚の慢性炎症」「成分分析による疾患診断」というキーワードのもとに集結させ、近年医学応用研究が著しく進んでいるラマン分光法を用いて慢性皮膚炎症疾患を評価する非侵襲非標識観察技術を開発することを目標とする。特に、乳幼児に多い食物アレルギーの発症予測や病状把握がラマン分光法により可能になれば、社会的意義は非常に大きい。また、本クラスター研究から期待される成果を基に、基本特許を取得し、日本医療研究開発機構(AMED)や科学技術振興機構(JST)が公募する事業への応募を行い外部資金の獲得を目指す。 |
| 研究概要図 | |
| 研究者の役割分担 | 髙成(研究総括):ファイバ型ラマン装置を用いた表皮の炎症・酸化ストレス標的物質の検出 南川:リモートプラズモニクス技術の検証、およびファイバ型装置のプローブへの実装 山本:アトピー性皮膚炎におけるリゾリン脂質を起因とする表皮バリア機能の検証 異島:ポリスルフィドによる皮膚・毛髪の抗酸化作用の検証 清水:経皮感作食物アレルギーモデル動物の作製、および表皮組織の病理学的検討 |
徳島大学の研究特集