| 研究期間 | 2018/4/1 - 2021/3/31 |
| 研究課題名 | 【終了】宇宙世代にむけたがん予防対策のための機能性食材と治療薬の開発 |
| カテゴリー | 全てのクラスター、研究クラスター一覧、医学、終了した研究クラスター、基礎、薬学、創薬、バイオ、生物、栄養、食品、ゲノム、バイオ |
| SDGs | 3.保健 9.イノベーション 10.不平等 |
| 応募課題 | |
| クラスター長氏名 | 岸本 幸治(大学院社会産業理工学研究部生物資源産業域、生物資源産業学域、講師) |
| 所属する研究者氏名 | 1. 二川 健(徳島大学大学院医歯薬学研究部 医科栄養学分野・教授) 2. 竹谷 豊 (徳島大学大学院医歯薬学研究部 医科栄養学分野・教授) 3. 土屋浩一郎(徳島大学大学院医歯薬学研究部 薬学域・教授) |
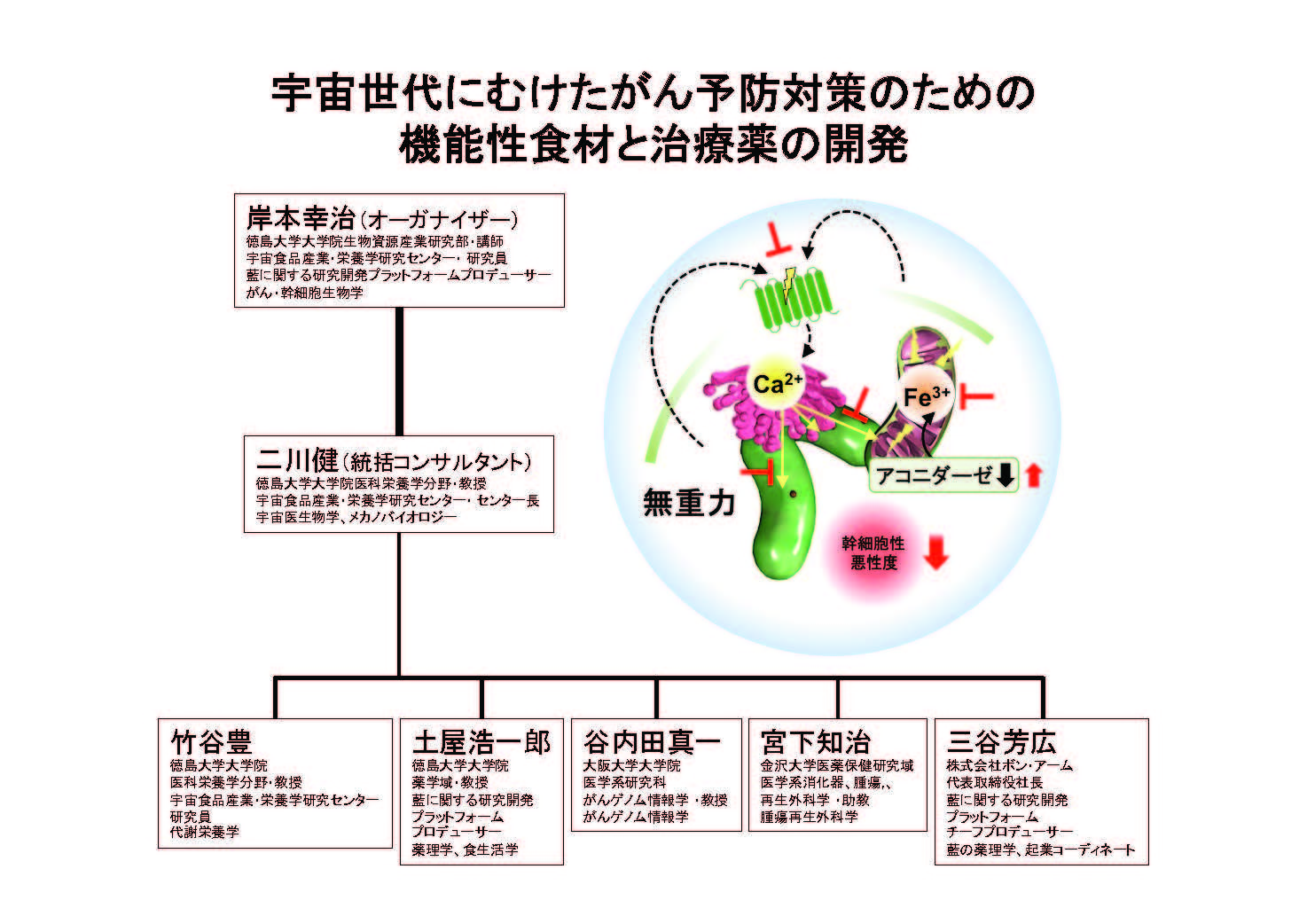
| 研究概要 | 申請者らは脳腫瘍細胞が酸化ストレスに曝露された環境(物理的シグナル)から産生される酸化脂質(化学的シグナル)を細胞膜表面受容体のG2Aが酸化ストレスセンサーとしての役割をはたし、腫瘍細胞の幹細胞性と悪性化の制御を行っていることを明らかにしてきた。一方、二川らは無重力(機械的ストレス)によるミトコンドリアと小胞体の相互作用からなるMAM構造(メカニカルストレスセンサー)の変化が酸化ストレスを発生し、筋萎縮や筋細胞傷害を起こすことを明らかにしている。脳腫瘍細胞の幹細胞性が還元剤やキレート剤で低下すること、幹細胞性の低下に伴いミトコンドリア膜電位やATP産生が低下する結果は、幹細胞性制御がミトコンドリアの鉄に起因していることを示唆している。一方、筋萎縮が見られるマウスの細胞内には鉄の蓄積がみられ、これは鉄シャペロンタンパク質の過剰発現によって回復することが示されている。すなわち、筋萎縮も鉄の蓄積によるミトコンドリア機能障害に起因していることが示唆される。これら両モデルの結果から、脳腫瘍細胞および筋細胞ではエネルギー代謝と鉄制御のマスターレギュレーターであるアコニダーゼが重力下および無重力下環境における細胞障害に対して重要な役割を果たしていると考えた。来る宇宙時代に備え、無重力空間での生活が発がんや腫瘍の悪性化に対してどのような影響をあたえるのかアコニターゼの機能を中心に、そのメカニズムを明らかにし、がん予防や抗腫瘍に貢献するエネルギー代謝および細胞内レドックスバランス機能を補完・調整する薬剤および機能性食材を開発することが本研究の目的である。 |
| 研究概要図 | |
| 研究者の役割分担 | 岸本幸治:無重力下での脳腫瘍細胞の幹細胞性獲得および悪性化におけるアコニダーゼの機能解析 二川 健 :無重力下でのミトコンドリア機能におけるアコニダーゼの役割解析 竹谷 豊:代謝物解析 土屋浩一郎: 抗酸化成分の同定 |
徳島大学の研究特集